المواد الذرّيّة
عائلة الموادّ الأخيرة التي سنتعرّف عليها في فصل المبنى والترابط هي عائلة الموادّ الذرّيّة.
إنّها عائلة مميّزة وسنتعرّف على بعض الموادّ التي تنتمي إليها ولكن ليس على جميعها.
نذكّركم بأنّ المواد الجُزَيئيّة (كالماء مثلًا H2O، حيث تكون ذرّات اللافلزات مرتبطة بروابط تساهميّة لتشكيل وحدة تُسمى جُزيء)، والأيونيّة (مثل ملح الطعام NaCℓ، حيث تُكوّن ذرّة فلزّ وهي الأيون الموجب وذرّة لافلزّ وهي الأيون السالب شبكة أيونيّة)، والفلزّيّة (كمادّة الفضّة Ag التي تتكوّن من أيونات موجبة في بحر من الإلكترونات غير المُتمركزة)، هي مواد يسهل نسبيًا التعرّف عليها. على عكس هذه الموادّ، فإنّ التعرّف على المادّة بناءً على تركيبتها الكيميائيّة يكون أكثر إشكاليّة في المواد الذرّية.
لهذا السبب علينا أن نتعرّف ونحفظ غيبًا أنّ كلّ من الموادّ التالية: الماس (C) ، الچرافيت (C) ، السيليكون (Si)، ثُنائي أكسيد السيليكون/الكوارتز SiO2 وكَربيد السيليكون SiC هي موادّ ذرّيّة.
هناك بالطبع موادّ أخرى تنتمي إلى هذه العائلة، ولكننا لن نتطرّق إليها.
ما هو المشترك بين جميع هذه المواد؟
جميع الموادّ الذرّيّة تشكّل مبنى ضخمًا حيث ترتبط فيه الذرّات ببعضها البعض بأربطة تساهميّة. يمكن القول أنّه بمثابة مبنى لا نهائيّ من الذرّات المرتبطة بشبكة من الأربطة التساهميّة العديدة، باستثناء الچرافيت الذي يتمتّع بمبنى أكثر تميّزًا. سنتطرّق إليه فيما بعد.
كما في العائلات الأخرى التي تعرّفنا عليها حتى الآن، صِفات الموادّ الذرّيّة مُشتقة من مبنى المادّة، من الأربطة الموجودة فيها ومن تركيبة ذرّاتها.
إذًا ما هي خصائص وصِفات الموادّ الذرّيّة؟
- على المستوى الميكروسكوبيّ، يمكن القول إنّ الموادّ الذرّيّة تتكوّن من ذرّات مرتبطة بأربطة تساهميّة قويّة جدًا وتشكّل شبكة تُسمّى الشبكة الذرّيّة.
بقيّة الخصائص والصِفات تتعلّق بالمستوى الماكروسكوبيّ للموادّ الذرّيّة.
- كلّ الموادّ الذرّيّة تكون صلبة في درجة حرارة الغرفة.
- الموادّ الذرّيّة لها درجات انصهار عالية جدًا. لِصَهرها يتطلّب الأمر، في بعض الأحيان، استخدام ضغط عالٍ جدًا.
مُقتطف من مقال “صائغو الماس للأبد” (تجّار ألماس للأبد) في موقع “نعناع” :
"الماس هو مادّة صلبة، وكأيّ مادّة صلبة، يمكن أن ينصهر أو أن يتسامى (يتحوّل إلى غاز إذا قمنا بتسخينه لدرجة حرارة كافية). الماس هو شكل من أشكال الكربون: تمامًا مثل الچرافيت الموجود في قلم الرصاص أو فحم الشواء. عند تسخين الماس في الهواء، سيحترق كأيّ قطعة فحم وينتج ثاني أكسيد الكربون. بدون الأكسجين، سيتبخّر الماس ويتحوّل إلى كربون غازيّ. عند تبريده في ظروف عاديّة، سيعود الغاز إلى حالته الصلبة، لكنّنا لن نحصل من جديد على الماس، بل على مادّة سوداء (چرافيت أو فحم) لا تصلح للاستخدام في المجوهرات. لكن إذا تعرّض لضغط عالٍ ودرجة حرارة 3600 درجة مئويّة تقريبًا، فمن الممكن بالفعل الحصول على "بركة" من الماس. قبل نحو أربع سنوات، نجح الباحث ماركوس كوندسون (Marcus Knudson) من المختبر الوطنيّ سانديا في إذابة الماس من خلال تسريع ألواح الماس الدقيقة إلى سرعة تفوق 100,000 كم/ساعة (ما يقارب 30 كيلومترًا في الثانية). بحث أنّ الموجة الصدميّة ولّدت لفترة قصيرة جدًّا ضغطًا يعادل 10 ملايين أتموسفيرا وأدّى إلى إذابته وتحوّله إلى سائل. بكلمات أخرى، نعم، يمكننا إذابة الماس، لكن... أليس هذا خسارة؟"
تمّ أخذّ النصّ المُرفق من موقع “نعناع” دون أن نُجري أيّ تغيير على النصّ. إليكم هاتان المُلاحظتان:
1. ليس من المتّبع أن نقول بأنّ المادّة الصلبة ستَسيل.
2. ثنائيّ أكسيد الكربون هو ثاني أكسيد الكربون.
- المواد الذرّيّة لا تذوب في أيّ مُذيبٍ
- المواد الذرّيّة غير موصِلة للتيّار الكهربائيّ باستثناء الچرافيت الذي يوصِل للتيّار الكهربائيّ في الحالة الصلبة بسبب مبناه الخاصّ. يحتوي الچرافيت، كما سنشرح فيما بعد، على سحابة إلكترونات غير مُتمركزة ومُتنقِّلة تسمح بالتوصيل الكهربائيّ.
الماس والچرافيت
هذان شكلان تآصُليّان لعنصر الكربون، في الواقع هما شكلان من أشكال عديدة أخرى.
الأشكال المُتآصلة هي مبانٍ مختلفة مصنوعة من العنصر ذاته (كالمتزامرات في المركّبات، وهي موادّ لها نفس الصيغة الجّزَيئيّة ولكن صيغة بنائيّة مُختلفة).
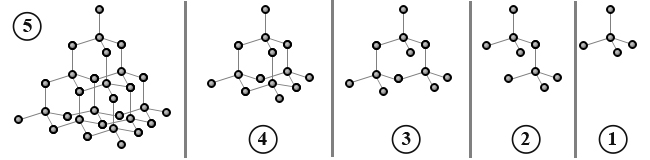
يتكوّن الماس من رباعيّات السطوح المترابطة فيما بينها. كلّ ذرّة كربون مرتبطة بأربع أربطة تساهميّة مع أربع ذرّات كربون أخرى وهكذا دواليك. المبنى حول كلّ ذرّة كربون هو مبنى رباعيّ السطوح. تمّ الحصول على مبنى قويّ جدًا ومستقرّ يمنح الماس الحقّ في أن يُسمّى المادّة الأقوى/الأصلب في الطبيعة.
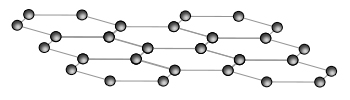
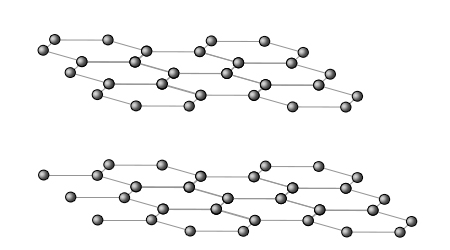
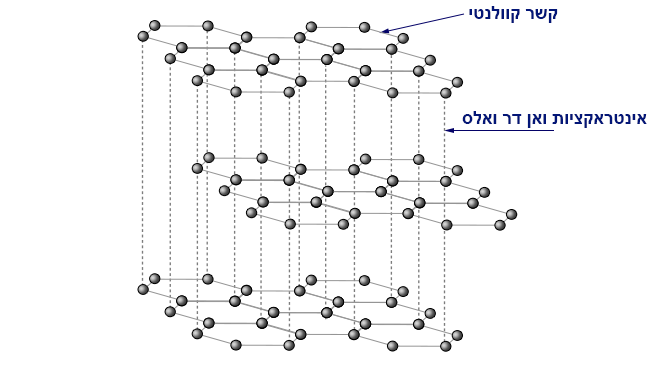
يتكوّن الچرافيت من طبقات من ذرّات الكربون. ترتبط كلّ واحدة منها بثلاث ذرّات كربون أخرى في رابط تساهميّ واحد، وبالتالي تتشكّل حلقات سداسيّة (كشكل خليّة النحل) من ذرّات الكربون. بما أنّ ذرّات الكربون تميل إلى تشكيل رابط تساهميّ بأربعة إلكترونات، وقد ذكرنا أنّه في مبنى الچرافيت ترتبط كلّ ذرّة كربون بثلاث ذرّات كربون أخرى فقط برابط تساهميّ واحد، ينشأ وضع يبقى فيه في كلّ ذرّة كربون إلكترون واحد غير مُزدوَج. جميع الإلكترونات غير المُزدوَجة في نفس الطبقة هي غير مُتمركزة وتتحرّك بشكل عشوائيّ فيها. هذه إلكترونات غير مُتمركزة وهي التي تسمح بمرور التيّار الكهربائيّ في الچرافيت في حالته الصلبة فقط. بين طبقة واحدة والأخرى هناك تأثيرات متبادلة ڤان در ڤالس التي يمكن فصلها بسهولة نسبيًا. لهذا السبب، يمكن الكتابة باستخدام الچرافيت (المادّة الموجودة في قلم الرصاص).
أنهينا فصل المبنى والترابط. فيما يلي درس يشمل جدولًا تلخيصيًا لصِفات المواد المختلفة ودرس آخر مع تمارين من أنواع مختلفة لتلخيص هذا الفصل.