בגרות בכימיה 2023
הוראות
- משך הבחינה: שלוש שעות
- מבנה השאלון ומפתח הערכה: בשאלון זה שני פרקים.
פרק ראשון – חובה – 40 נקודות
פרק שני – 60 נקודות (3×20 נקודות)
סה”כ – 100 נקודות - חומר עזר מותר בשימוש:
- מחשבון ( כולל מחשבון גרפי).
- דפי נוסחאות ונתונים (מצורפים).
- הוראות מיוחדות:
- בפרק הראשון יש תשע שאלות.
בכל אחת מהשאלות 1-8 מוצגות ארבע תשובות, ומהן יש לבחור בתשובה הנכונה. את התשובות הנכונות יש לסמן בתשובון שבסוף מחברת הבחינה (עמוד 19).
בשאלה 9 יש לענות על כל הסעיפים. - בפרק השני יש חמש שאלות. יש לענות על שלוש מהן.
- בפרק הראשון יש תשע שאלות.
יש לכתוב במחברת הבחינה בלבד. יש לרשום “טיוטה” בראש כל עמוד המשמש טיוטה.
כתיבת טיוטה בדפים שאינם במחברת הבחינה עלולה לגרום לפסילה.
השאלות בשאלון זה מנוסחות בלשון רבים, אף על פי כן על כל תלמידה וכל תלמיד להשיב עליהן באופן אישי.
בהצלחה!
השאלות
פרק ראשון (40 נקודות)
ענו על כל השאלות 1 – 8.
אם תענו נכון על שבע שאלות לפחות, תקבלו את מלוא 20 הנקודות.
לפני שתענו, קראו את כל התשובות המוצעות.
לכל שאלה מוצעות ארבע תשובות. בחרו בתשובה הנכונה.
* את התשובה שבחרתם סמנו בתשובון שבכריכה הפנימית בסוף מחברת הבחינה (עמוד 19).
* בכל שאלה סמנו בעט X במשבצת שמתחת לאות (א – ד) המייצגת את התשובה שבחרתם.
* בכל שאלה יש לסמן X אחד בלבד.
* כדי למחוק סימון יש למלא את כל המשבצת כך: ■
* אסור למחוק בטיפקס.
* שימו לב: כדאי להימנע ככל האפשר ממחיקות בתשובון, לכן מומלץ לסמן את התשובות הנכונות קודם בשאלון עצמו, ורק אחר כך לסמן אותו בתשובון.
- בטבלה שלפניכם מוצגים נתונים על ההרכב של שלושה חלקיקים שמסומנים באופן שרירותי באותיות X, Y, Z.
החלקיק מספר פרוטונים מספר נויטרונים היערכות אלקטרונים X 18 18 2,8,8 Y 17 18 2,8,8 Z 18 20 2,8,8 מהי הקביעה הנכונה?
- המטען של הגרעין בחלקיקים X ו- Y הוא זהה.
- לכל אחד משלושת החלקיקים X, Y, ו-Z אין מטען חשמלי.
- החלקיקים X ו- Z הם איזוטופים של אותו יסוד.
- שלושת החלקיקים X, Y ו- Z הם אטומים של יסודות שונים.
- לפניכם הנוסחאות המולקולריות של ארבע מולקולות: CℓCN , CO2, C2Cℓ2 , CS2.
המבנה של כל אחת מן המולקולות הוא קווי.
לפניכם ארבעה היגדים, א-ד, בעניין הקשרים הקוולנטיים במולקולות וקוטביות המולקולות.
מהו ההיגד הנכון?- בכל המולקולות, כל הקשרים הקוולנטיים הם קוטביים.
- המולקולות C2Cℓ2 ו- CO2 הן קוטביות.
- במולקולות CS2 ו- CO2 יש קשרים קוולנטיים יחידים.
- במולקולות CℓCN ו- C2Cℓ2 יש קשר קוולנטי משולש.
- ערבבו בכוס כימית 200 מ”ל תמיסת נתרן כלורי, NaCℓ(aq), בריכוז 0.4M,
עם 200 מ”ל תמיסת אלומיניום כלורי, AℓCℓ3(aq), בריכוז 0.4M.
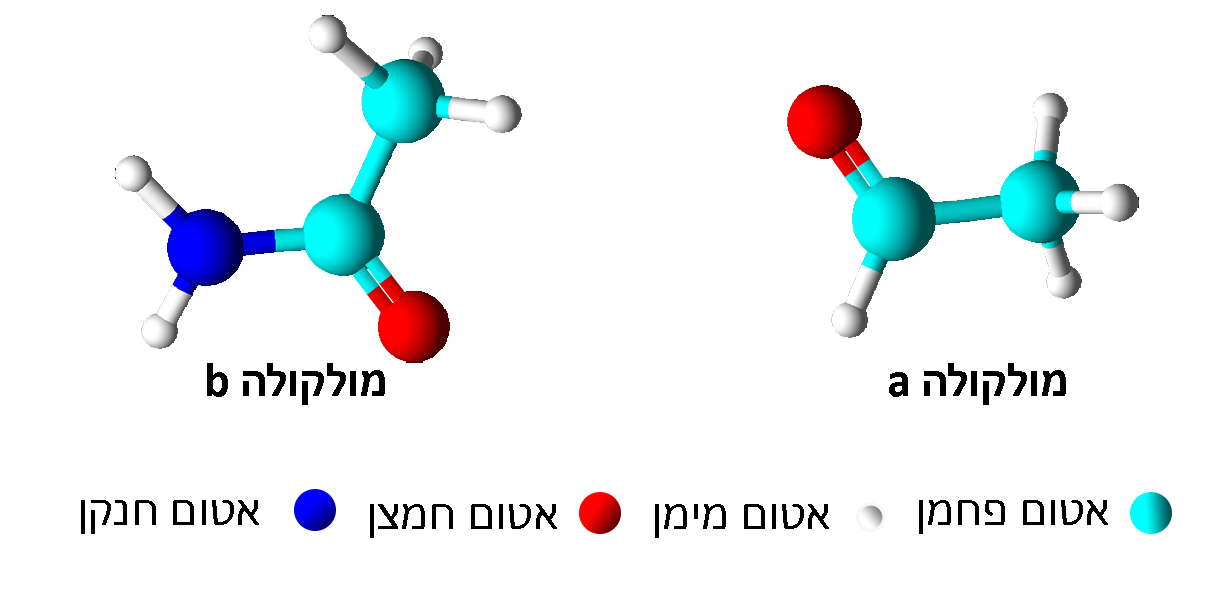
מהו הריכוז המולרי של כל אחד מן היונים בתמיסה שהתקבלה בתום הערבוב?Cℓ¯(aq) Aℓ3+(aq) Na+(aq) א. 0.8M 0.2M 0.2M ב. 0.8M 0.4M 0.4M ג. 0.4M 0.4M 0.4M ד. 0.2M 0.2M 0.2M - המודלים שלפניכם מייצגים את נוסחאות המבנה של שתי מולקולות המסומנות באופן שרירותי a ו- b.
 לפניכם ארבעה היגדים I-IV.
לפניכם ארבעה היגדים I-IV.
I. במולקולה a הקבוצה הפונקציונלית היא קטון.
II. במולקולה b הקבוצה הפונקציונלית היא אמיד.
III. בין מולקולות a עשויים להיווצר גם קשרי מימן.
iV. בין מולקולות b עשויים להיווצר גם קשרי מימן.
מה הם ההיגדים הנכונים?- I ו- II
- II ו- III
- I ו- IV
- II ו- IV
- שעוות הנרות עשויה בעיקר מפחמימן שנוסחתו המולקולרית היא C25H52 (מסה מולרית: ).
לפניכם תגובת השרפה המלאה של אדי הפחמימן בעת בעירת הנר:
C25H52(g) + 38O2(g) → 25CO2(g) + 26H2O(g)
נמצא שכמות האנרגייה שנפלטה בתגובת השרפה של 1.76 גרם C25H52(g) שווה ל- 77.825kJ.
מהו שינוי האנתלפיה התקנית, ΔH0, בתגובת השרפה של 1 מול C25H52(g)?- 15,565kJ+
- 15,565kJ-
- 77,825kJ+
- 77,825kJ-
- לפניכם התגובות (1) – (3):
(1) C(s) + 2H2(g) → CH4(g) ΔH01 = -74.8kJ
(2) C(s) + 2H2(g) + O2(g) → CH3OH(ℓ) ΔH02 = -238.9kJ(3) CH4(g) + O2(g) → CH3OH(ℓ) ΔH03 =?
מהו ערכו של ΔH03 עבור תגובה (3)?
- 313.7kJ-
- 313.7kJ+
- 164.1kJ-
- 164.1kJ+
- תלמידים ערכו כמה ניסויים, ובהם הם טבלו פסים של 3 מתכות שונות בתמיסות המכילות יוני מתכות. בכל ניסוי הם טבלו פס של מתכת אחת בתמיסה מימית שהכילה יונים של מתכות אחרות (וגם יונים שליליים).
בטבלה שלפניכם מצוין בנוגע לכל אחד מן הניסויים אם התרחשה בו תגובה (+) או שלא התרחשה בו תגובה (-).יוני מתכות
מתכות
Ba2+(aq) Zn2+(aq) Pb2+(aq) בריום Ba(s) + + אבץ Zn(s) – + עופרת Pb(s) – – מהו הסדר הנכון של יוני המתכות על פי כושרם לחמצן?
- Zn2+(aq) > Pb2+(aq) > Ba2+(aq)
- Ba2+(aq) > Zn2+(aq) > Pb2+(aq)
- Pb2+(aq) > Zn2+(aq) > Ba2+(aq)
- Pb2+(aq) > Ba2+(aq) > Zn2+(aq)
- לכלי פתוח המכיל תמיסה של חומצה גופרתית, H2SO4(aq), מכניסים מגנזיום, Mg(s).
כל המתכת טבולה בתמיסה.
לפניכם ניסוח נטו של התגובה המתרחשת.Mg(s) + 2H3O+(aq) → Mg2+(aq) +H2(g) +H2O(ℓ)
לפניכם רשימת משתנים הקשורים לניסוי:
I. מסת גז המימן.
II. שטח הפנים של המגנזיום.
III. ריכוז תמיסת החומצה הגופרתית.
IV. נפח הכלי שבו מתרחשת התגובה.אילו מן המשתנים ברשימה עשויים להשפיע על קצב התגובה?
- I ו- II
- II ו- III
- III ו- IV
- I ו- IV
ניתוח קטע ממאמר מדעי – חובה
- קראו את הקטע שלפניכם, וענו על כל הסעיפים שאחריו לפי ההנחיות (שאלת חובה – 20 נקודות).
התחממות גלובלית – השינוי מתחיל בקטבים
ההתחממות של אזורי הקטבים בכדור הארץ מתרחשת מהר מכפי שחזו מדענים, והיא מעידה על שינוי האקלים בעולם.
אחת התוצאות של התחממות זו היא הפשרה מהירה של קרחונים יבשתיים בגרינלנד, אי הקרוב לקוטב הצפוני, ובאנטרטיקה, בקוטב הדרומי. הפשרת הקרחונים היבשתיים גורמת, נוסף על עליית פני הים, גם לשינוי מסלולי סופות באזורים של אמריקה הצפונית.
קרחון יבשתי (glacier) הוא מצבור גדול וקדום של קרח שנוצר במשך אלפי שנים משכבות השלג שירדו והתגבשו זו על גבי זו. הקרחון שנוצר על פני היבשה גדל לאורך השנים ונע באיטיות לכיוון הים. הקרחונים היבשתיים מהווים מקור חשוב ועיקרי למי שתייה במקומות רבים בכדור הארץ.
קרחון יבשתי מכיל 99% קרח, H2O(s), וכ- 1% זיהומים שונים מן הים ומן האוויר הכוללים יונים כגון: נתרן, Na+, מגנזיום, Mg2+, סידן, Ca2+, כלור, Cℓ−, ויוניים גופרתיים, SO42-. מקורם של היונים בתרכובות יוניות שונות שהתמוססו במים. מסת יוני הנתרן ב- 1 ק”ג קרחון היא 0.4×10-6 גרם.
בעקבות התחממות האטמוספרה בעת האחרונה, מתחממים גם מי האוקיינוסים בקצב עולה. לפיכך מותך בסיס הקרחון היבשתי הנמצא קרוב לים המתחמם, וחלקים גדולים ממנו נופלים למים. חלקי הקרחון היבשתי שנופלים למים הופכים לקרחונים ימיים צפים (icebergs), שניתכים ובמשך הזמן גורמים לעליית פני הים.
שלג וקרח הם חומרים לבנים שמחזירים את רוב קרינת השמש אל החלל. מי האוקיינוס הכהים יותר קולטים את קרינת השמש ומתחממים. לכן להפשרת חלק מהקרחונים השפעה כפולה:
– מסת המים, היכולים לקלוט קרינה ולהתחמם, גדלה.
– מסת הקרח, המחזיר את קרינת השמש אל החלל ומונע התחממות, קטנה.
בעקבות עליית טמפרטורת האוויר והפשרת הקרחונים, האוויר בקטבים מכיל אדי מים רבים יותר, יש יותר ענני גשם ולכן נפוצות יותר סערות גשם מלוות בברקים.
ענני גשם מכילים מספר עצום של מולקולות מים. עקב תנועתן של מולקולות המים, עובר זרם אלקטרונים באוויר בין העננים או בין הענן לקרקע, והוא הופך את המולקולות שבאוויר לחלקיקים טעונים ולאטומים בודדים. מעבר אלקטרונים זה כרוך בפליטת אנרגייה רבה הגורמת לטמפרטורת האווויר בסביבה הקרובה לעלות ל- 30,000°C.
עקב מעבר האנרגייה רואים ברק, הבזק לבן ובוהק, ושומעים רעם שנוצר מהתפשטות מהירה של האוויר המתחמם.
כימאים גילו כי במהלך היווצרות הברקים אפשר לגלות באוויר אטומי חמצן ואטומי מימן בודדים, שמקורם במולקולות המים שבעננים. יש ברקים שפוגעים בחומרים דליקים הנמצאים על פני האדמה וגורמים לעיתים קרובות לשרפות.
הידע על השינויים המתחוללים בעולמנו והבנתם מאפשר למדענים לחזות את השפעות האקלים ולהיערך מבעוד מועד למנוע פגיעה בחיים ולצמצם נזקים.
מקור:
https://climate.nasa.gov/news/3062/warming-seas-are-accelerating-greenland-glacier-retreat/
| ענו על הסעיפים א, ב, ד, ה, ו, ז ועל אחד מן הסעיפים ג או ח |
- רשמו נוסחאות של 4 תרכובות יוניות העשויות להיות מקור ליונים שיש בקרחונים.
בצפון כדור הארץ ריכוז יוני הנתרן במי ים הוא 0.46.
- פי כמה גדולה המסה של יוני הנתרן ב- 1 ליטר מי ים לעומת המסה של יוני הנתרן ב- 1 ק”ג קרחון? פרטו את חישוביכם.
| סעיף ג הוא סעיף בחירה. אם תבחרו לענות עליו אל תענו על סעיף ח |
- המודל בתרשים שלפניכם מייצג קטע של סידור מולקולות המים בקרח.
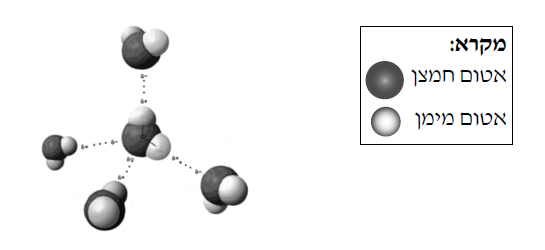
- התבוננו במודל וקבעו לכמה אטומי מימן קשור כל אטום חמצן ובאילו סוגי קשרים.
- נסחו את תהליך ההיתוך של הקרח.
- לפניכם שני היגדים I ו- II. קבעו עבור כל היגד אם הוא נכון או לא נכון.
- לאטומים של מולקולות המים בקרח יש אופני תנועה מסוג תנודה בלבד.
- למולקולות המים בקרח יש אופני תנועה מסוג מעתק בלבד.
- קבעו אם תהליך ההיתוך של הקרח בקרחון יבשתי הוא תהליך אנדותרמי או אקסותרמי.
הסבירו ובססו את תשובתכם על סוגי הכוחות הפועלים בין המולקולות. - קרחון שמסתו 2 טון נפל למים והותך כולו. כמה מולקולות מים נוספו לים? פרטו חישוביכם.
נתון: 1 טון = 1×106 גרם. - לפניכם שלושה היגדים I, II ו- III. התבססו על המאמר המדעי וקבעו עבור כל אחד מן ההיגדים אם הוא נכון או לא נכון.
- בעת התרחשות ברק נשברים קשרים קוולנטיים בין האטומים במולקולות המים הנמצאות בעננים.
- בעת התרחשות ברק נשברים קשרים קוולנטיים בין האטומים במולקולות הנמצאות באוויר.
- ברק משפיע על הטמפרטורה של הסביבה רק כאשר הוא פוגע באדמה.
| סעיף ח הוא סעיף בחירה. אם תבחרו לענות עליו אל תענו על סעיף ג |
- לפניכם גרף אנרגייה סכמטי עבור 1 מול מים.
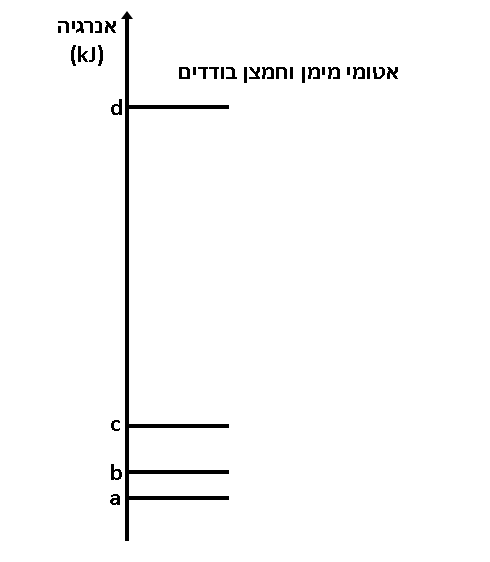
- מהו מצב הצבירה של המים בכל אחד מהמצבים: a, b, c?
- הסבירו מדוע מעבר אנרגייה d-c גדול ממעבר האנרגייה b-a.
פרק שני (60 נקודות)
ענו על שלוש מן השאלות 14-10 (לכל שאלה 20 נקודות).
10. מבנה האטום, מבנה וקישור, חישובים
סוללות ליתיום מספקת אנרגייה למכשירים רבים. הן מכילות תרכובות יוניות, תמיסות שמכילות יונים ניידים וחומרים נוספים.
ליתיום, Li(s), היה מרכיב חיוני בסוללות הליתיום הראשונות.
- תארו את מבנה הליתיום, Li(s), והסבירו מדוע החומר מוליך חשמל בטמפרטורת החדר.
בסוללות שאינן מבוססות על ליתיום הממס הוא מים. אולם, בסוללות ליתיום הממסים אינם מימיים.
לפניכם התגובה הבאה:
Li(s) + H2O(ℓ) → H2(g) + Li+(aq) +OH–(aq) ΔH0 <0
- הסבירו מדוע לא משתמשים במים כממס בסוללת ליתיום.
אחד הממסים בסוללת ליתיום הוא די-מתיל קרבונט (DMC).
לפניכם ייצוג מקוצר לנוסחת המבנה של מולקולת DMC:
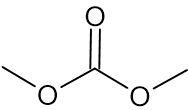
- רשמו נוסחה מולקולרית של DMC.
לפניכם ייצוגים מקוצרים לנוסחאות מבנה של שלוש מולקולות נוספות: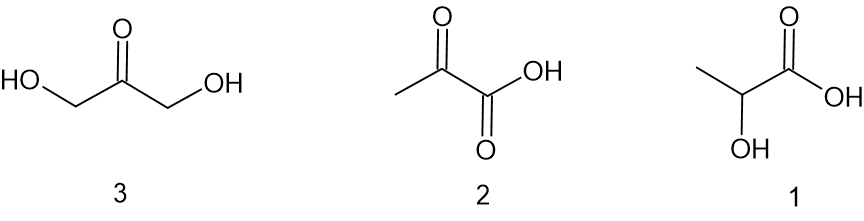
- איזו מולקולה או אילו מולקולות הן איזומרים של DMC? הסבירו את בחירתכם.
- טמפרטורת הרתיחה של DMC נמוכה מטמפרטורת רתיחה של מים באותם תנאים. הסבירו עובדה זו.
- המסו 139 גרם DMC במים והכינו 1 ליטר תמיסה.
- הסבירו מדוע DNC מתמוסס במים.
- חשבו את הריכוז המולרי של התמיסה שהוכנה.
סוללות ליתיום נטענות נקראות סוללות ליתיום-יון והן משמשות, בין השאר, להפעלת מכוניות חשמליות.
יש סוללות ליתיום-יון שמבוססות על תרכובות של ליתיום, כגון ליתיום קובלט חמצני, LiCoO2(g).
התרכובת היונית LiCoO2(g) מורכבת מיוני ליתיום, יוני קובלט, Co3+, ויוני חמצן, O2-.
- רשמו נוסחאות ייצוג אלקטרונים של יוני ליתיום ושל יוני חמצן.
11. חומצות שומן, מבנה וקישור, חישובים
בפולי קקאו יש חמאת קקאו ומוצקי קקאו. חמאת קקאו מכילה שומן. מוצקי קקאו מכילים חומרים שאינם שומן.
לאחר טיפול מתאים בפולי הקקאו מייצרים מהם שוקולד.
שוקולד הוא תערובת של חמאת קקאו ומוצרי קקאו ומרכיבים אחרים כמו סוכר וחומרי טעם במינונים שונים.
בחמאת קקאו יש טריגליצרים שמורכבים בעיקר משלוש חומצות השומן שמוצגות בטבלה 1:
| חומצת שומן | סמל | ייצוג מקוצר לנוסחת מבנה |
| חומצה פלמיטית | P | 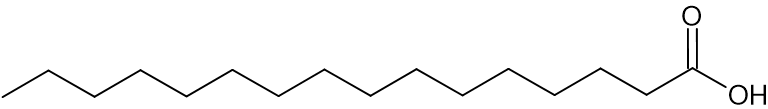 |
| חומצה סטארית | S | |
| חומצה אולאית | O |
טבלה 1
- כתבו רישום מקוצר של כל אחת מחומצות השומן שמוצגות בטבלה 1.
- טמפרטורת ההיתוך של חומצה פלמיטית נמוכה מטמפרטורת ההיתוך של חומצה סטארית. מהו הגורם לכך?
חמאת קקאו מכילה חומצות שומן נוספות בכמויות קטנות, ובהן חומצות השומן שרשומות בטבלה 2:
| חומצת שומן | רישום מקוצר של חומצת השומן |
| חומצה מיריסטית | C14:0 |
| חומצה לינולאית | C18:2ω6 cis, cis |
| חומצה לינולנית | C18:3ω3 cis, cis, cis |
| חומצה אראכידית | C20:0 |
טבלה 2
- רשמו ייצוג מקוצר של נוסחאות המבנה של חומצות השומן הלא רוויות שרשומות בטבלה 2.
- טמפרטורת ההיתוך של חומצה אולאית גבוהה מטמפרטורת ההיתוך של חומצה לינולאית. מהו הגורם לכך?
חומצת שומן נוספת בחמאת הקקאו היא חומצה פלמיטולאית. הרישום המקוצר של חומצה זו הוא C16:1ω7 cis.
- רשמו ייצוג מלא של נוסחת המבנה של מולקולת חומצה פלמיטולאית.
הסמלים של הטריגליצרידים בחמאת קקאו הם: POP, SOS, POS.
לפניכם ייצוג מקוצר לנוסחת המבנה של מולקולת טריגליצריד
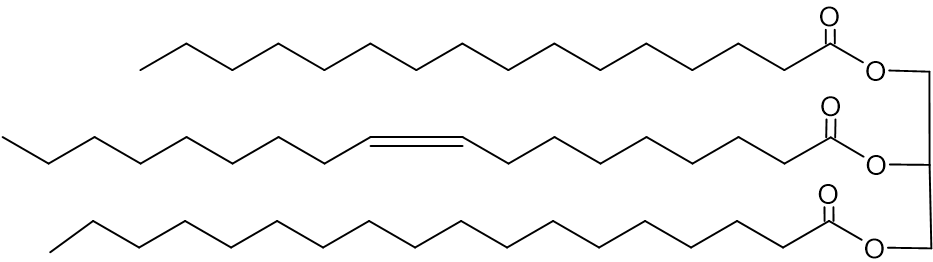
- בחרו את הסמל המתאים לייצוג המקוצר של נוסחת המבנה הנתונה.
לפניכם ייצוג מקוצר של נוסחת המבנה של שלוש מולקולות:
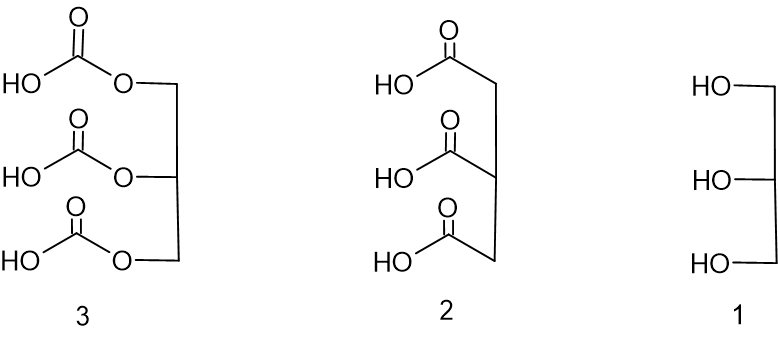
- איזה ייצוג מקוצר משלושת הייצוגים האלה מתאים לייצוג המקוצר של נוסחת המבנה של מולקולת הגליצרול?
מוצקי הקקאו שבשוקולד מכילים, בין השאר, את החומרים הממריצים תאוברומין וקפאין.
לפניכם ייצוג מקוצר של נוסחאות המבנה של מולקולת תאוברומין, C7H8N4O2, ומולקולת קפאין, C8H10N4O2.

- הסבירו מדוע החומרים תאוברומין וקפאין מתמוססים בחמאת קקאו.
- לפניכם נתונים על ריכוז קפאין במשקאות שונים.
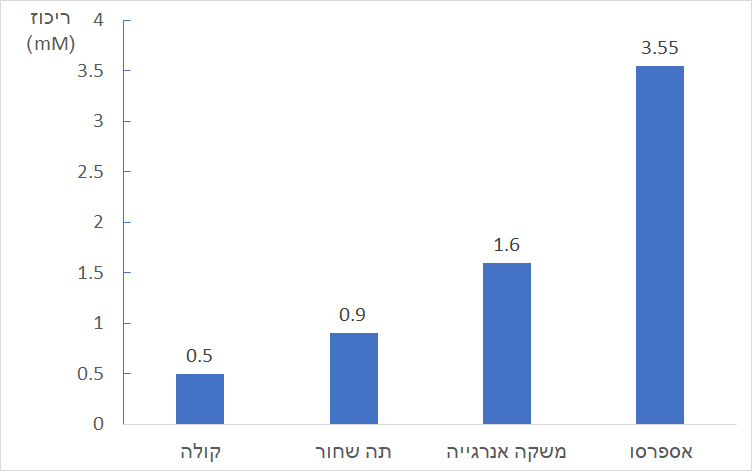
רצוי לצרוך לא יותר מ- 400 מיליגרם קפאין ביום. תלמיד שתה 4 פחיות משקה אנרגייה ביום אחד.- מהי מסת הקפאין בפחית אחת של משקה אנרגייה? פרטו את חישוביכם.
- קבעו אם התלמיד עבר את צריכת הקפאין היומית המומלצת (בהנחה שמשקה זה היה מקור הקפאין היחיד). פרטו את חישוביכם.
נתונים: 1×10-3M = 1mM
1 מיליגרם = 10-3×1 גרם
נפח פחית = 330 מ”ל
12. חומצות ובסיסים
לפניכם 3 כוסות כימיות שכל אחת מהן מכילה חומצה אחרת.

בכל אחת מן התמיסות טבלו נייר לקמוס ורוד וגם נייר לקמוס כחול. כמו כן, בדקו בכל אחת מהתמיסות את ערך ה- pH ואת המוליכות החשמלית.
בכל אחת מן הכוסות נמצא כי:
- הצבע של שני ניירות הלקמוס בתמיסה הוא ורוד.
- ערך ה- pH של התמיסה הוא 2.
- התמיסה מוליכה חשמל.
נתון: בטבלה שלפניכם מצויין הצבע של ניירות לקמוס שנטבלו בתמיסות שונות.
| בתמיסה חומצית | בתמיסה ניטרלית | בתמיסה בסיסית | |
| נייר לקמוס ורוד | אין שינוי | אין שינוי | משנה גוון לכחול |
| נייר לקמוס כחול | משנה גוון לוורוד | אין שינוי | אין שינוי |
- א
- ציינו את כל סוגי החלקיקים שנמצאים בכל אחת מן התמיסות בכוסות 3-1.
- מדוע כל אחת מהתמיסות מוליכה חשמל?
- מדוע ערך ה- pH זהה בכל הכוסות?
לכל אחת מן הכוסות הוסיפו תמיסת נתרן הידרוקסידי, NaOH(aq), בנפחים ובריכוזים שונים, כמפורט לפניכם.
לכוס 1 – הוסיפו 50 מ”ל תמיסת NaOH(aq) בריכוז 0.02M.
לכוס 2 – הוסיפו 50 מ”ל תמיסת NaOH(aq) בריכוז 0.01M.
לכוס 3 – הוסיפו 100 מ”ל תמיסת NaOH(aq) בריכוז 0.02M.
לאחר ההוספה, התקבלה תמיסה צלולה בכל אחת מן הכוסות.
בכל אחת מן הכוסות טבלו נייר לקמוס ורוד.
- ב
- רשמו ניסוח נטו של התגובה שהתרחשה בכל אחת מן הכוסות.
- באיזו מן הכוסות נראה שינוי בצבע של נייר הלקמוס? פרטו את חישוביכם.
- קבעו אם ה- pH היה קטן מ- 7, שווה ל- 7, או גדול מ- 7 בכל אחת מן הכוסות לאחר ההוספה של תמיסת נתרן הידרוקסידי.
- נערכו שני ניסויים
ניסוי 1
מדדו את ה- pH של 100 מ”ל תמיסת H2SO4(aq) בריכוז 0.2M.
לתמיסה זו הוסיפו 100 מ”ל תמיסת HCℓ(aq) בריכוז 0.2M וערבבו את שתי התמיסות.
בתום הערבוב בדקו שוב את ה- pH.- קבעו אם בתום הערבוב ה- pH גבוה מן ה- pH ההתחלתי, נמוך ממנו או שווה לו. נמקו או פרטו את חישוביכם.
ניסוי 2
מדדו את ה- pH של 100 מ”ל תמיסת HCℓ(aq) בריכוז 0.1M.
לתמיסה זו הוסיפו 100 מ”ל תמיסת NaCℓ(aq) בריכוז 0.1M וערבבו את שתי התמיסות.
בתום הערבוב בדקו שוב את ה- pH.
- קבעו אם בתום הערבוב ה- pH גבוה מן ה- pH ההתחלתי, נמוך ממנו או שווה לו? נמקו או פרטו את חישוביכם.
13. חמצון־חיזור, מבנה וקישור וחישובים
השאלה עוסקת במתכת טיטניום, Ti(s), ובסגסוגות שלה. למתכת זו ולסגסוגות שלה יש שימושים רבים בתעשייה, בין היתר בתעשיית התעופה והחלל.
להפקת טיטניום משתמשים במחצבים המכילים טיטניום חמצני TiO2(s).
הפקת המתכת טיטניום מתבצעת בשני שלבים:
שלב ראשון
בשלב זה טיטניום חמצני, TiO2(s), מגיב עם פחמן, C(s), ועם גז כלור, Cℓ2(g).
אחד התוצרים הוא הנוזל, TiCℓ4(ℓ), על פי תגובה (1)
(1) TiO2(s) + C(s) + Cℓ2(g) → TiCℓ4(ℓ) + CO2(g)
שלב שני
התרכובת הנוזלית טיטניום ארבע כלורי, TiCℓ4(ℓ), שנוצרה בתגובה (1), מגיבה עם מגנזיום מתכתי, Mg(s), על פי תגובה (2).
(2) TiCℓ4(ℓ) + 2Mg(s) → Ti(s) + 2MgCℓ2(s)
נתון: אלקטרושליליות של טיטניום, Ti – 1.54.
- קבעו מי החומר המחמצן ומי החומר המחזר בכל אחת מן התגובות (1) ו- (2). נמקו את קביעתכם.
- איזו מתכת מחזרת טובה יותר – מגנזיום או טינטניום? נמקו את תשובתכם.
- כמה טון טיטניום חמצני, TiO2(s), דרושים כדי להפיק טון אחד של המתכת טיטניום, Ti(s)? פרטו את חישוביכם.
נתון: 1 טון = 106 × 1 גרם - אחת הסגסוגות השימושיות בתעשיית החלל והתעופה נוצרת מעיבוד של המתכות טיטניום, Ti(s), ונדיום, V(s), ואלומיניום, Aℓ(s).
בכל 100 גרם סגסוגת כזאת יש 90 גרם טיטניום, 4 גרם ונדיום והשאר אלומיניום.- לפניכם רשימה של סוגי חלקיקים: אטומים, מולקולות, יונים, יונים ניידים, אלקטרונים ניידים.
אילו סוגי חלקיקים מרשימה זו מרכיבים את הסגסוגת? - כמה מול אלומיניום יש ב- 1 ק”ג סגסוגת זו? פרטו את חישוביכם.
- לפניכם רשימה של סוגי חלקיקים: אטומים, מולקולות, יונים, יונים ניידים, אלקטרונים ניידים.
כאשר מכינים סגסוגת של טיטניום צריך להתיך אותו. טיטניום מותך יכול להגיב עם גזים שבאוויר.
- בתגובה בין טיטניום מותך ובין גז חנקן, N2(g), שבאוויר נוצרת התרכובת טיטניום חנקני, TiN(s).
נסחו ואזנו את התגובה. - מעבדים את הטיטניום המותך בסביבה של גז ארגון, Ar(g). הסבירו מדוע.
- בסעיפי השאלה הוזכרו החומרים: Ti(s), TiO2(s), TiCℓ4(ℓ), TiN(s).
קבעו באיזה מן החומרים האלה הטיטניום יכול להגיב רק כמחזר.
14. מבנה וקישור, חמצון־חיזור, חומצות ובסיסים
בטבלה שלפניכם מצוינים נתונים של שלושה יסודות המסומנים באופן שרירותי באותיות: c, b, a.
| סמל שרירותי של היסוד | טמפרטורת ההיתוך של היסוד (C°) | טמפרטורת הרתיחה של היסוד (C°) | הולכה חשמלית של היסוד בטמפרטורת החדר |
| a | 98 | 883 | מוליך |
| b | 259- | 253- | לא מוליך |
| c | 7- | 59 | לא מוליך |
- התאימו בין היסודות: מימן, H2(g), ברום, Br2(ℓ), נתרן, Na(s) ובין האותיות c, b, a.
- ב
- קבעו מהו סוג הקשרים בין אטומי היסוד המסומן באות b.
- הסבירו מדוע טמפרטורת הרתיחה של היסוד המסומן באות c גבוהה מטמפרטורת הרתיחה של היסוד המסומן באות b.
בתנאים מתאימים היסודות מגיבים ביניהם.
- בתגובה בין היסוד שסומן באות a ובין היסוד שסומן באות b מתקבל תוצר יחיד שהוא מוצק בטמפרטורת החדר.
מהי דרגת החמצון של כל אחד מן החלקיקים בתוצר שהתקבל? - בתגובה בין היסוד שסומן באות a ובין היסוד שסומן באות c מתקבל תוצר יחיד שהוא מוצק בטמפרטורת החדר.
תוצר זה מסיס במים.- נסחו את תגובת ההמסה במים של התוצר.
- האם התמיסה הנוצרת מוליכה חשמל? נמקו את תשובתכם.
- בתגובה בין היסוד שסומן באות b ובין היסוד שסומן באות c מתקבל תוצר יחיד, שהוא גז בטמפרטורת החדר.
תוצר זה מגיב עם מים ונוצרת תמיסה.- מהי נוסחת התוצר?
- נסחו את תגובת התוצר עם מים.
- האם התמיסה הנוצרת חומצית, בסיסית, או ניטרלית? נמקו את תשובתכם.
- היסוד חנקן, N2(g), מגיב עם היסוד המסומן באות b, ומתקבל תוצר יחיד שהוא גז. תוצר זה מגיב עם מים ויוצר תמיסה בסיסית.
- נסחו את התגובה לקבלת התוצר.
- נסחו את התגובה בין התוצר המתקבל ובין מים.
- היסוד חנקן, N2(g), מגיב עם היסוד המסומן באות a, ומתקבל תוצר יחיד.
רשמו את נוסחת התוצר בטמפרטורת החדר.
בהצלחה!