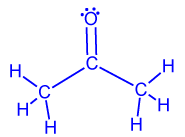
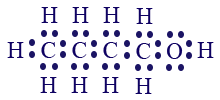المادّة الجُزَيئيّة والمادّة الأيونيّة تمرين
تعلّمنا حتّى الآن في فصل المبنى والترابط عن عائلتين من الموادّ: الموادّ الأيونيّة والموادّ الجُزَيئيّة سنقوم بتلخيص هاتَين العائِلَتين مع تمرين في الموضوع.
- مُعطى جدول يحتوي على مُعطيات حول عدد من الموادّ::
المادّة درجة الغليان (C°) التوصيل الكهربائيّ في المادّة الصلبة التوصيل الكهربائيّ في المُنصهر (السائل) التوصيل الكهربائيّ في المحلول المائيّ الذائبيّة في الماء نوع الشبكة (أيونيّة أم جُزَيئيّة) المادّة A 117.7 – – – + B 1533 – + – – C 77 – – – – D 19- – – – + E 1381 – + + + F 78 – – – +
كما مُعطاة الصيغ للموادّ التالية:
RbCℓ, C4H9OH, CCℓ4, AgBr, CH2O, C2H5OH
من المعروف أنّ خليط الـ AgBr مع الماء مُعكّر، في حين أنّ خليط الـ RbCl مع الماء صافٍ.
- أكمِلوا الجدول.
| المادّة | درجة الغليان (C°) | التوصيل الكهربائيّ في المادّة الصلبة | التوصيل الكهربائيّ في المُنصهر (السائل) | التوصيل الكهربائيّ في المحلول المائيّ | الذائبيّة في الماء | نوع الشبكة (أيونيّة أم جُزَيئيّة) | החומר |
| A | 117.7 | – | – | – | + | جُزيئيّة | C4H9OH |
| B | 1533 | – | + | – | – | أيونيّة | AgBr |
| C | 77 | – | – | – | – | جُزيئيّة | CCℓ4 |
| D | 19- | – | – | – | + | جُزيئيّة | CH2O |
| E | 1381 | – | + | + | + | أيونيّة | RbCℓ |
| F | 78 | – | – | – | + | جُزيئيّة | C2H5OH |
فيما يلي الشرح للمُطابقة:
يُمكننا أن نُلاحظ وجود مادّتين أيونيّتين بناءً على تركيب العناصر فيها. هذه هي الموادّ التي تحتوي على فلزّات ولافلزّات (أيونات فلزّية موجبة وأيونات لافلزّيّة سالبة). جميع الموادّ الأخرى في القائمة، التي تحتوي صيغتها على ذرّات لعناصر لافلزّيّة فقط، هي موادّ جُزَيئيّة.
AgBr و-RbCℓ هي مواد أيونيّة. كلاهما موصلان للتيّار الكهربائيّ في الحالة المنصهرة لأنّهما في هذه الحالة يحتويان على أيونات مُتنقّلة. لذلك، فإنهما يتطابقان مع الموادّ B و- E.
وفقًا لمُعطيات السؤال، فإنّ المادّة AgBr تُشكّل خليطًا مُعكّرًا في وجود الماء، ممّا يشير إلى أنّها لا تذوب بشكل جيّد في الماء. لذلك فهي المادّة B، بينما المادّة المُتبقّية RbCl هي المادّة E. من بين الموادّ الجُزَيئيّة في السؤال، ذابت ثلاث مِنها في الماء وواحدة لم تذوب. تتمتّع المادّتان C4H9OH ו-C2H5OH بقدرةٍ على تكوين أربطة هيدروجينيّة بين الجُزَيئات وبينما يوجد في المادّة CH2O موقع لتكوين أربطة هيدروجينيّة بين جُزّيئاتها وبين الهيدروجين المكشوف من الإلكترونات في جُزَيء الماء. لهذا السبب، فإنّ هذه المواد الثلاثة تذوب في الماء. المادّة الوحيدة التي لا تذوب في الماء بسبب وجود التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئاتها ولا موقع لديها لتكوين أربطة هيدروجينيّة هي CCℓ4 وبالتالي هي المادّة C.
بين الموادّ الثلاثة المُتبقّية C4H9OH, C2H5OH ו- CH2O نميّز بينها بمساعدة الفروقات في درجة غليانها.
بين جُزَيئات المادّة C4H9OH توجد تأثيرات متبادلة ڤان در ڤالس وأربطة هيدروجينيّة. سحابة الإلكترونات فيها أكبر من سحابة الإلكترونات في الماّدتين المتبقّيتين، وبالتالي فإنّ القوى بين الجُزَيئات فيه أقوى. لهذا السبب، درجة غليانها أعلى من درجة غليان المادّتين الأخرتين. لذلك هو المادّة A.
الموادّ المُتبقّية هي C2H5OH ו-CH2O. بين جُزَيئات المادّة C2H5OH توجد أربطة هيدروجينيّة وتأثيرات متبادلة ڤان در ڤالس. بين جُزَيئات المادّة CH2O توجد فقط تأثيرات متبادلة ڤان در ڤالس وسحابة الإلكترونات فيها أصغر مُقارنةً بسُحب الإلكترونات في المادّة C2H5OH. لذلك، التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئاتها أكثر ضعفًا وبالتالي درجة غليان الـ CH 2O أقلّ. للمادّة-C2H5OH درجة غليان أعلى بسبب وجود أربطة هيدروجينيّة بين جُزَيئاتها، بالإضافة إلى تأثيرات متبادلة ڤان در ڤالس. الخُلاصة هي، المادّة C2H5OH هي F والمادّة CH2O هي D.
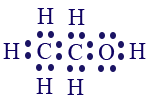
- اكتبوا صيغة التمثيل الإلكترونيّ لجُزَيئات الموادّ الجُزَيئيّة التي وجدتموها في الجدول أعلاه.
- اشرحوا لماذا يذوب CH2O في الماء. صيغوا عمليّة الإذابة وارسموا رابطًا بين جُزَيء الماء وجُزَيء CH2O.
المادّة CH2O هي مادّة جُزَيئيّة توجد بين جُزَيئاتها تأثيرات متبادلة ڤان در ڤالس. لكن لديه نقطة (ذرّة أوكسجين) لتكوين أربطة هيدروجينيّة مع ذرّات الهيدروجين المكشوفة من الإلكترونات في جُزَيء الماء. فيما يلي صيغة عمليّة الإذابة في الماء:
رسم الرابط بين جُزَيء الماء وجُزَيء الـ CH2O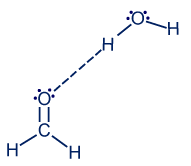
- لماذا تكون درجة غليان المادّة المطابقة لـ A أعلى من درجة غليان المادّة المطابقة لـ F؟ علِّلوا إجابتكم.
المادّتان A – C4H9OH ו-F – C2H5OH هما موادّ جُزَيئيّة توجد بين جُزَيئاتها أربطة هيدروجينيّة وتأثيرات متبادلة ڤان در ڤالس. من حيث الأربطة الهيدروجينيّة، في الجُزَيئين يوجد عدد النقاط ذاته لتكوين الأربطة الهيدروجينيّة، ولكن بما أنّ الجزء الهيدروكربونيّ (الجزء الهيدروفوبيّ) للمادةّ A أكبر منه في المادّة F (أي أنّ لها سحابة إلكترونات أكبر)، فإن احتمال تكوين ثنائيّ تقاطُب لحظيّ على الجُزَيئات أكبر، وبالتالي تكون الشحنات الجُزئيّة الناتجة أكبر. لذلك، التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئات المادّة A أقوى. نحتاج إلى طاقة أكبر لتفكيك التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئات الـ C4H9OH ودرجة غليانها أعلى.
- اكتبوا صيغة لعمليّة الإذابة في الماء للمادّة التي تطابق صيغتها المادّة E. اشرحوا لماذا يتمتّع المحلول بخاصيّة التوصيل الكهربائيّ.
فيما يلي صيغة عمليّة الإذابة في الماء
المحلول موصلٌ للتيّار الكهربائيّ لأنّه يحتوي على أيونات مٌتنقّلة.
- اشرحوا لماذا درجة غليان المادّة التي تطابق صيغتها المادّة C أعلى من درجة غليان المادّة التي تطابق صيغتها المادّة D.
المادّة C هي CCℓ4 والمادّة D هي CH2O. المادّتان هما مادّتان جُزَيئيّتان. بين جُزَيئات المادّتين هناك تأثيرات متبادلة ڤان در ڤالس. بما أنّ سحابة الإلكترونات في جُزَيئات المادّة C أكبر من سحابة الإلكترونات في جُزَيئات المادّة D، هناك احتمال أكبر لتكوين ثنائيّات تقاطُب لحظيّة على الجُزَيئات، والشحنات الجزئيّة الناتجة أكبر. لذلك، التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئات المادّة C أقوى. لذلك، نحتاج إلى طاقة أكبر لتفكيك التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئات المادّة C. وبالتالي، فإنّ درجة غليان المادّة C أعلى.
- المادّة C لا تذوب في الماء. اشرحوا السبب بناءً على صيغة المادّة التي حدّدتموها.
المادّة C هي CCℓ4. وهي مادّة جُزَيئيّة توجد بين جُزَيئاتها تأثيرات متبادلة ڤان در ڤالس. الماء هو مادّة جُزَيئيّة توجد بين جُزَيئاتها أربطة هيدروجينيّة. لذلك، لا تتكوّن تأثيرات متبادلة ڤان در ڤالس (لا تتكوّن أربطة) بين جُزَيئات المادّة C وبين جُزَيئات الماء.
- اشرحوا لماذا المادّة التي تطابق صيغتها المادّة B موصلة للكهرباء في الحالة المنصهرة. صيغوا عمليّة انصهار المادّة.
المادّة التي تطابق صيغتها المادّة B هي المادّة الأيونيّة AgBr. في الحالة المنصهرة، يكون له أيونات مُتنقّلة وبالتالي يوجد توصيل كهربائيّ.
صياغة عمليّة الانصهار هي
- مُعطى جدول يحتوي على مُعطيات حول عدد من الموادّ:
المادّة درجة الغليان (C°) لتوصيل الكهربائي في المادّة الصلبة لتوصيل الكهربائيّ في المُنصهر (السائل) التوصيل الكهربائيّ في المحلول المائيّ الذائبيّة
في الماءنوع الشبكة (أيونيّة أم جُزَيئيّة) المادّة A 56 – – – + B 218 – – – – C 210 – + + + D 77 – – – – E 150 – – – + F 97 – – – + مُعطى أيضًا قائمة الموادّ التالية:
(CH3)2CO, H2O2, CCℓ4, NH4NO3, CHI3, C3H7OH
- أكمِلوا الجدول.
| المادّة | درجة الغليان (ºC) | لتوصيل الكهربائي في المادّة الصلبة | لتوصيل الكهربائيّ في المُنصهر (السائل) | التوصيل الكهربائيّ في المحلول المائيّ | الذائبيّة في الماء | نوع الشبكة (أيونيّة أم جُزَيئيّة) | المادّة |
| A | 56 | – | – | + | جُزيئيّة | (CH3)2CO | |
| B | 218 | – | – | – | – | جُزيئيّة | CHI3 |
| C | 210 | – | + | + | + | أيونيّة | NH4NO3 |
| D | 77 | – | – | – | – | جُزيئيّة | CCℓ4 |
| E | 150 | – | – | – | + | جُزيئيّة | H2O2 |
| F | 97 | – | – | – | + | جُزيئيّة | C3H7OH |
- اكتبوا صياغة لعمليّات الإذابة في الماء للموادّ NH4NO3 ו- H2O2. كيف يمكنكم التمييز بين المحاليل؟ ماذا ستفعلون وماذا ستجدون؟
صياغة عمليّة الإذابة في الماء:
يُمكننا التمييز بين المحاليل من خلال فحص التوصيل الكهربائيّ. محلول المادّة NH4NO3(s) موصلٌ للتيّار الكهربائيّ لأنّه يحتوي على أيونات مٌتنقّلة.
- اشرحوا لماذا درجة غليان المادّة B أعلى من درجة غليان المادّة D؟
الموادّ (B) CHI3 ו-(D) CCℓ4 هي موادّ جُزَيئيّة توجد بين جُزَيئاتها تأثيرات متبادلة ڤان در ڤالس. لأنّ جُزَيئات الـ CHI3 لها سحابة إلكترونات أكبر والجُزَيئات قُطبيّة، فإنّ التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئاتها أقوى من التأثيرات المتبادلة ڤان در ڤالس بين جُزَيئات الـ CCℓ4. لذلك، نحتاج إلى طاقة أكبر لتفكيك هذه الروابط ودرجة غليانها أعلى.
- للمادّة التي تطابق صيغتها المادّة E درجة غليان أعلى من درجة غليان الماء (100°C). اشرحوا السبب.
المادّة التي تطابق صيغتها المادّة E هي H2O2. هو مادّة جُزَيئيّة توجد بين جُزَيئاتها أربطة هيدروجينيّة. الماء أيضًا هو مادّة جُزَيئيّة توجد بين جُزَيئاتها أربطة هيدروجينيّة. نظرًا لأنّ جُزَيء H2O2 يحتوي على العديد من النقاط لتكوين أربطة هيدروجينيّة، تنتج المزيد من الأربطة الهيدروجينيّة بين جُزَيئاته وبالتالي تكون أقوى من الأربطة الهيدروجينيّة بين جُزَيئات الماء . لذلك، نحتاج إلى طاقة أكبر لتفكيك الروابط بين جُزَيئات الـ H2O2 ودرجة غليانه أعلى.
- اكتبوا التمثيل الكامل للصيغة البنائيّة للمادّة (CH3)2CO.
- للمادّتين CHI3 ו-CCℓ4 مبنى رُباعيّ السطوح. حدّددوا لكلّ منها ما إذا كانت قطبيّة (تملك ثنائيّ قطب ثابت). علِّلوا إجابتكم.
CHI3 هي مادّة قُطبيّة لأنّ جُزَيئاتها ليست ذات بُنية مُتماثلة. إذ حدث عدم تماثُل في سحابة الإلكترونات. المادّة CCℓ4 هي مادّة غير قُطبيّة لأنّ جُزَيئاتها ذات بُنية مُتماثلة. لا يحدُث عدم تماثُل في سحابة الإلكترونات.
- استعينوا بقائمة المجموعات الوظيفيّة (تجدونها في درس المجموعات الوظيفيّة) واذكروا أيّ المجموعات الوظيفيّة توجد في الموادّ المختلفة الواردة في قائمة الموادّ في بداية السؤال.
هناك مادّتان لهما مجموعات وظيفيّة:
المادّة C3H7OH التي تحتوي على مجموعة كحوليّة OH—
في المادّة (CH3)2CO توجد مجموعة كيتونيّة